Nat Commun | 浙江大学赵经纬团队与鞠振宇、舒有生、陈厚早团队合作揭示β-NMN延缓髓鞘老化并增强髓鞘修复的新机制
发布单位:衰老与再生医学研究院 发布时间:2022-03-09
在中枢神经系统(central nervous system, CNS)中,髓鞘(myelin)是由少突胶质细胞(oligodendrocyte, OL)形成的、包绕神经轴突的节段样结构,是神经冲动快速传导的结构基础,参与神经信号的编码并为神经轴突提供营养支持。衰老过程中髓鞘出现特征性结构变化即髓鞘老化(myelin aging),被认为是CNS衰老的重要驱动力。OL胞体或者髓鞘受损引起的髓鞘变性称为脱髓鞘(demyelination),而广泛分布于CNS内的成年神经干细胞之一-少突胶质细胞前体细胞(oligodendrocyte progenitor cell, OPC)可以分化为成熟的OL,形成新的髓鞘包裹轴突,这一再生过程称为复髓鞘(remyelination)。研究表明,伴随衰老引起的髓鞘修复能力下降与衰老的OPC分化能力下降密切相关。因此,靶向干预老年OPC分化是探索延缓髓鞘老化、促进脱髓鞘疾病的复髓鞘治疗新方法的重要策略之一。
Sirtuins是高度保守的烟酰胺腺嘌呤二核苷酸(nicotinamide adenine dinucleotide, NAD+)依赖的去乙酰化酶,哺乳动物中sirtuin家族有7个亚型(SIRT1-SIRT7),我们发现其中只有SIRT2特异性地在OL谱系中高表达。目前鲜有关于SIRT2在髓鞘发育或者髓鞘再生过程中的研究,且仅有的研究结果还存在争议,具体分子机制仍不清楚。
2022年3月9日,浙江大学医学院赵经纬教授团队,与暨南大学衰老与再生医学研究院鞠振宇教授、复旦大学脑科学转化研究院舒友生教授及中国医学科学院北京协和医学院陈厚早教授等合作在Nature Communications在线发表题为Restoring nuclear entry of Sirtuin 2 in oligodendrocyte progenitor cells promotes remyelination during ageing的研究论文。该论文采用端粒酶功能障碍早衰小鼠、SIRT2全身敲除和条件敲除小鼠,综合多种研究手段,发现了补充NAD+的直接前体β-烟酰胺单核苷酸(β-NMN),可以促进老年OPC中SIRT2的表达和入核,进而增强老年OPC的分化和延缓髓鞘老化,以及髓鞘损伤后的修复。该研究深入揭示了NAD+的靶向分子、入核机制及表观遗传机制。

该研究首先确认了SIRT2在OPC中的表达,其表达模式随着髓鞘发育过程从大多数在OPC的细胞核转变为主要在成熟OL的细胞质。通过构建脱髓鞘小鼠模型,作者检测到在髓鞘修复过程中,SIRT2重新在OPC中表达并入核,且随衰老下降。为进一步探究SIRT2与髓鞘修复之间的关系,作者使用SIRT2-/-小鼠和NG2CreERT; SIRT2fl/fl小鼠(仅在OPC中特异敲除SIRT2),构建局部脱髓鞘模型,结果发现小鼠的复髓鞘效率明显降低,证明OPC中的SIRT2在髓鞘修复过程中发挥着至关重要的作用。
少突胶质细胞是高度耗能的细胞,然而OPC的代谢组学随着衰老如何变化尚不清楚。作者纯化分离了早衰小鼠(G3 Terc-/-)的OPC,采用代谢质谱技术检测到衰老OPC中NAD+含量显著下降。补充β-NMN使SIRT2的表达上调并提高了衰老OPC的分化能力。在体实验中,作者在早衰小鼠和自然衰老小鼠胼胝体中均发现了髓鞘老化和髓鞘修复效率降低现象。而补充β-NMN使SIRT2在OPC中的表达和核定位均增加,并可以改善髓鞘结构质量,延缓髓鞘老化并增强髓鞘修复;在功能上,作者通过电生理检测到补充β-NMN可以促进胼胝体复髓鞘区轴突的信号传导。
接下来,作者在SIRT2-/-小鼠中证实SIRT2在NAD+促进髓鞘修复中发挥着必不可少的作用,并进一步解析了其分子机制:补充β-NMN促进OPC中SIRT2的重新表达及其入核。SIRT2入核可以使H3K18去乙酰化,进而抑制ID4的转录,促进MBP的转录,进而促进OPC的分化,最终延缓髓鞘的老化,改善老年髓鞘的损伤修复(如下图所示)。
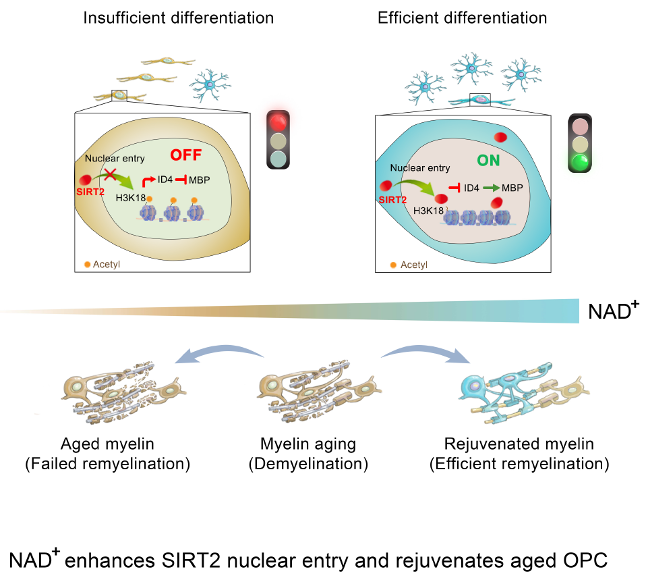
综上,该论文揭示了补充β-NMN可以提高老年OPC中SIRT2的表达和入核,从而促进老年OPC的分化,延缓髓鞘老化并改善髓鞘损伤修复的具体作用机制。本研究为预防中枢神经系统髓鞘老化提供了重要的理论基础,并为脱髓鞘疾病治疗的临床转化提供了新的分子靶点和候选药物。
赵经纬教授为本文最后通讯作者, 鞠振宇教授、舒友生教授及陈厚早教授为共同通讯作者。浙江大学医学院博士研究生马晓茹和杭州师范大学基础医学院朱栩栋教授为本文共同第一作者。本研究受到国家科技部重点研发计划、国家自然科学基金委员会等项目资助。
赵经纬课题组致力于探索促进少突胶质细胞前体细胞的增生及分化的新策略、揭示脑老龄化的分子机制研究,期望为修复受损的髓鞘和延缓脑衰老提供新思路。在研项目包括国家级重大项目及重点项目。欢迎新近或即将毕业的相关专业的博士生申请博士后!
实验室详细信息见:
https://person.zju.edu.cn/jwzhaoatzjuion
